พันธะโควาเลนต์กับพันธะไอออนิก

เนื้อหา
- สารบัญ: ความแตกต่างระหว่างพันธะโควาเลนต์กับพันธะไอออนิก
- แผนภูมิเปรียบเทียบ
- พันธบัตรโควาเลนท์คืออะไร
- อิออนบอนด์คืออะไร
- ความแตกต่างที่สำคัญ
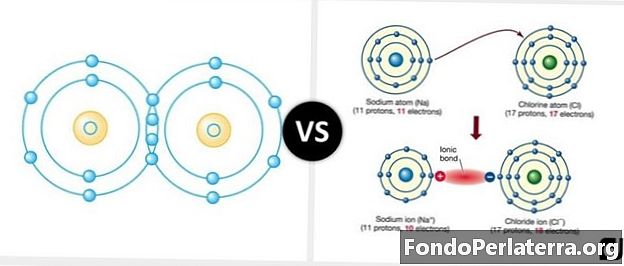
ความแตกต่างที่สำคัญระหว่างพันธะไอออนิกและพันธะโควาเลนต์คือการแบ่งปันคู่อิเล็กตรอนและอะตอม ในพันธะโควาเลนต์อะตอมจะถูกดึงดูดด้วยไฟฟ้าสถิตในขณะที่อยู่ในพันธะไอออนิก คู่อิเล็กตรอนจะถูกใช้ร่วมกันระหว่างอะตอม
สารบัญ: ความแตกต่างระหว่างพันธะโควาเลนต์กับพันธะไอออนิก
- แผนภูมิเปรียบเทียบ
- พันธบัตรโควาเลนท์คืออะไร
- อิออนบอนด์คืออะไร
- ความแตกต่างที่สำคัญ
- คำอธิบายวิดีโอ
แผนภูมิเปรียบเทียบ
| พื้นฐานของความแตกต่าง | พันธะโควาเลนต์ | พันธะไอออนิก |
| คำนิยาม | พันธะโควาเลนต์เป็นพันธะเคมีชนิดหนึ่งที่เกี่ยวข้องกับการแบ่งปันคู่ที่ใช้ร่วมกันหรือคู่พันธะ (อิเล็กตรอนคู่) ระหว่างอะตอม | พันธะไอออนิกเป็นชนิดของพันธะเคมีที่เกี่ยวข้องกับการแบ่งปันหรือการรวมอิเลคตรอนหนึ่งหรือหลายอะตอมโดยอะตอมหนึ่งไปยังอะตอมอื่น |
| การเกิดขึ้น | พันธะโควาเลนต์เป็นผลมาจากปฏิสัมพันธ์ของอะตอมที่เป็นกลาง | พันธะอิออนเป็นผลมาจากการมีปฏิสัมพันธ์ระหว่างแอนไอออนและไพเพอร์ |
| ศักยภาพทางเคมี | นี่เป็นพันธะเคมีที่ค่อนข้างอ่อนแอ | สิ่งเหล่านี้เป็นพันธะเคมีที่แข็งแกร่งที่สุด |
| รูปแบบ | องค์ประกอบที่ไม่ใช่โลหะก่อให้เกิดพันธะโควาเลนต์ | องค์ประกอบโลหะจากพันธะไอออนิก |
| สถานะอิเล็กตรอน | อิเล็กตรอนที่ใช้ร่วมกัน | การถ่ายโอนอิเล็กตรอนทั้งหมด |
| สถานะของสสาร | ของเหลวและก๊าซที่อุณหภูมิห้อง | ของแข็งที่อุณหภูมิห้อง |
| สารประกอบ | อินทรีย์ | นินทรีย์ |
| การละลาย | ไม่ละลายในน้ำ | ละลายในน้ำ |
| รูปร่าง | รูปร่างที่แน่นอน | ไม่มีรูปร่างแน่นอน |
| การตั้งชื่อ | คำนำหน้าภาษากรีก | เลขโรมัน |
| ตัวอย่าง | กรดไฮโดรคลอริกและมีเทน | กรดซัลฟูริกและโซเดียมคลอไรด์ |
พันธบัตรโควาเลนท์คืออะไร
พันธะโควาเลนต์หรือที่รู้จักกันในชื่อพันธะโมเลกุลคือชนิดของพันธะเคมีที่เกี่ยวข้องกับการแบ่งปันของคู่ที่ใช้ร่วมกันหรือคู่พันธะ (คู่อิเล็กตรอน) ระหว่างอะตอม ในโมเลกุลส่วนใหญ่อิเล็กตรอนที่ใช้ร่วมกันอนุญาตให้แต่ละอะตอมได้รับเปลือกนอกเต็มรูปแบบซึ่งสอดคล้องกับโครงแบบอิเล็กทรอนิกส์ที่เสถียร หากอะตอมมีความสัมพันธ์ใกล้ชิดกันกับอิเล็กตรอนพันธะโควาเลนต์ก็น่าจะเกิดขึ้นเพราะความสัมพันธ์แบบเดียวกันกับอิเล็กตรอนและไม่มีแนวโน้มที่จะบริจาคโดยอะตอม อะตอมใช้อิเล็กตรอนร่วมกันในการกำหนดค่าออคเต็ตและมีความเสถียรและแข็งแกร่งยิ่งขึ้น เนื่องจากปฏิสัมพันธ์ของซิกม่าและไพริเบตส์พันธะโควาเลนต์สามารถสร้างพันธะสี่ประเภทคือแบบเดี่ยวคู่สามและสี่เท่า อะตอมออกซิเจนเป็นตัวอย่างที่ดีที่สุดที่ต้องการอิเล็กตรอนสองตัวเพิ่มเติมเพื่อสร้างเปลือกปิดในขณะที่อะตอมไฮโดรเจนต้องการหนึ่งในรูปแบบเปลือกปิด อะตอมออกซิเจนแบ่งปันอิเล็กตรอนสองตัวกับอะตอมไฮโดรเจนดังนั้นอะตอมของทั้งคู่จึงมีเปลือกปิด ในที่สุดสิ่งนี้จะสร้างโมเลกุลของน้ำ
อิออนบอนด์คืออะไร
พันธะไอออนิกเป็นชนิดของพันธะเคมีที่เกี่ยวข้องกับการแบ่งปันหรือการรวมอิเลคตรอนหนึ่งหรือหลายอะตอมโดยอะตอมหนึ่งไปยังอะตอมอื่น พันธะอิออนเป็นผลมาจากองค์ประกอบเหล่านั้นที่สูญเสียอิเล็กตรอนอย่างง่ายดายและองค์ประกอบเหล่านั้นที่ได้รับอิเล็กตรอน พันธบัตรประเภทนี้ไม่ได้มีไว้สำหรับโมเลกุลเนื่องจากการปฏิสัมพันธ์ระหว่างประจุตามกฎหมายของคูลอมบ์ พันธะไอออนิกยังคงแข็งที่อุณหภูมิห้องเพราะในระหว่างการโปรยของไอออนที่มีประจุหลายพันล้านครั้งไอออนแต่ละไอออนจะถูกล้อมรอบด้วยไอออนที่มีประจุต่างกัน สถานที่น่าสนใจไฟฟ้าสถิตระหว่างประจุลบและประจุบวกจะจับสารประกอบเข้าด้วยกัน พลังงานโดยรวมในระหว่างกระบวนการพันธะไอออนิกนั้นเป็นค่าบวกแสดงให้เห็นว่าปฏิกิริยานั้นเป็นความร้อนและไม่เอื้ออำนวย ในทางกลับกันปฏิกิริยานี้เป็นที่นิยมในเวลาเดียวกันเพราะการดึงดูดไฟฟ้าสถิตของพวกเขา ตัวอย่างทั่วไปของพันธะไอออนิกคือโซเดียมหรือเกลือ อะตอมโซเดียมให้อิเล็กตรอนอย่างรวดเร็วซึ่งจะส่งผลให้ประจุบวก คลอรีนยอมรับอิเล็กตรอนเหล่านี้และมีประจุเป็นลบ อะตอมทั้งสองที่มีประจุตรงข้ามกันจะดึงดูดกันเพื่อสร้างโมเลกุลโซเดียมคลอไรด์
ความแตกต่างที่สำคัญ
- ในพันธะโควาเลนต์วงโคจรของอิเล็กตรอนจะทับซ้อนกันในขณะที่อิออนพันธบัตรแยกออกจากกัน
- พันธะโควาเลนต์ค่อนข้างอ่อนเมื่อเทียบกับพันธะไอออนิกที่แข็งและเปราะ
- ทั้งอะตอมของโลหะและอะตอมที่ไม่ใช่โลหะมีส่วนเกี่ยวข้องในการก่อตัวของพันธะไอออนิกในขณะที่อยู่ในรูปของพันธะโควาเลนต์ มีเพียงอะตอมที่ไม่ใช่โลหะเท่านั้นที่มีส่วนเกี่ยวข้อง
- พันธะโควาเลนต์เกิดขึ้นเนื่องจากการแบ่งปันอิเล็กตรอนในขณะที่การเกิดพันธะไอออนิกเกิดขึ้นเนื่องจากการถ่ายโอนอิเล็กตรอน
- โมเลกุลเป็นอนุภาคในพันธะโควาเลนต์ในระหว่างการเกิดสารประกอบในขณะที่อิออนในพันธะเหล่านี้จะมีประจุเป็นบวกและมีประจุเป็นลบ
- พันธะโควาเลนต์ไม่ใช่ตัวนำในขณะที่พันธะอิออนิกเป็นตัวนำ
- พันธะโควาเลนต์เกิดขึ้นระหว่างอะตอมที่แตกต่างกันเล็กน้อยในอิเลคโตรเนกาติวีตี้ พันธะไอออนิกเกิดขึ้นระหว่างอะตอมที่มีความแตกต่างอย่างมากในอิเลคโตรเนกาติวีตี้
- พันธะไอออนิกนั้นต้องการจุดหลอมเหลวสูงและจุดเดือดในกรณีที่มีพันธะไอออนิก พันธะโควาเลนต์ต้องการจุดหลอมเหลวและจุดเดือดต่ำในกรณีที่พันธะโควาเลนต์
- มีเทนและกรดไฮโดรคลอริกเป็นตัวอย่างทั่วไปของโควาเลนต์โซเดียมคลอไรด์และกรดซัลฟูริกเป็นตัวอย่างของพันธะไอออนิก
- พันธะโควาเลนต์มีรูปร่างที่แน่นอนในขณะที่พันธะไอออนิกไม่มีความแน่นอน
- พันธะโควาเลนต์มีขั้วต่ำในขณะที่พันธะไอออนิกมีขั้วสูง
- โมเลกุลโควาเลนต์ 100% จะละลายในน้ำมัน แต่ไม่ใช่ในน้ำในขณะที่พันธะไอออนิกจำนวนมากมีความสามารถในการละลายในน้ำ แต่ไม่ใช่ในน้ำมัน
- พันธะโควาเลนต์มีความสำคัญเนื่องจากโมเลกุลของคาร์บอนมีปฏิกิริยากับพันธะโควาเลนต์เป็นหลักในขณะที่พันธะไอออนิกมีความสำคัญเพราะสิ่งเหล่านี้ช่วยให้การสังเคราะห์สารประกอบอินทรีย์จำเพาะ
- พันธะโควาเลนต์สามารถเป็นได้ทั้งองค์ประกอบและสารประกอบในขณะที่พันธะไอออนิกสามารถเป็นสารประกอบได้เท่านั้น